(Göster / Gizle) Sunum İçeriği: Düz metin (text) olarak..
1. Sayfa
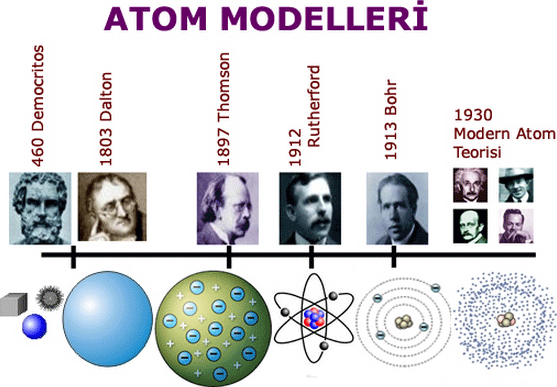
Thomson ModeliRutherford ModeliBohr ModeliKuantum ModeliAtom Modelleri
2. Sayfa
AtomI. Bütün maddeler atomlardan oluşmuştur.II. Materyallerin özellikleri (Renk, sertlik, doku v.s.) şunlara bağlıdırB) Atomların nasıl düzenlendiğiA) Hangi tür atomlardan meydana geldiğiKarbon atomları veFarklı dizilişleri
3. Sayfa
Bugünki Teknoloji (Top-down technology)Nanoteknoloji nedir?Cisimler kesilerek isten şekil verilirNanoteknoloji (Bottom-up technology)Atomlar bir araya getirilerek daha büyük cisimler elde edilebilir..Grafit ElmasKumBilgisayarCan we do this now??? Not Yet, but…..
4. Sayfa
Katot IşınlarıYa yükler aynı, buna karşılık kütle H den daha azYa da tanecik kütlesi H ile aynı, fakat yükü daha azCathode RaysElektronların Keşfi ve ÖzellikleriJ.J. Thomson (1897)e/m = 1.75882 108 coulomb/g Katot ışınları negatif yüke sahiptir. Katot ışınları manyetik ve elektrik alanda saparlar. Yük/kütle oranı (e/m) katot materyalinin cinsine bağlı değildir.
5. Sayfa
Thomson Atom ModeliBu model geçerli bir süre kaldı. Ta ki……Thomson’un öğrencisi Rutherford bazı deneyler yapana kadar…. “plum pudding model” Atom elektrikçe nötral olmalıdır. Yüklerin sallanması ışımaya neden olur. Farklı elementler farklı elektron sayısına sahiptir.
6. Sayfa
Rutherford’un Saçılma Deneyi (1910)Çekirdeğin çapı atomundakinden yaklaşık 100,000 kez daha küçüktür.1. Atomlarda büyük boşluklar bulunur.2. Atomun kütlesi çok küçük bir çekirdekte yoğunlaşmıştır.3. Çekirdek pozitif yüklüdür.
7. Sayfa
Rutherford Atom ModeliPlanetary Model“Planetary Model” Gezen ve yıldızlara benzerAtomların ışıma spektrumlardaki frekansların elektronların dairesel hareket frekanslarının katları olması beklenir. Atomların ışıma spektrumlarını açıklayamaz.Maxwell teorisine göre bütün hareket halindeki yüklü taneciklerelekromanyetik ışıma yapar. Sürekli enerji kaybeden elektron gittikçe yavaşlayıp sonunda çekirdeğe düşmesi gerekir, yani yaşayamazlar.Atomların varoluşlarını açıklayamaz.
8. Sayfa
Balmer SerisiJ. Balmer (1885) H atomunun GB spektrumundaki hatların frekanslarına uyan aşağıdaki bağıntıyı vermiştir.n = 3, 4, 5,.... Rydberg, Balmer modelini bütün spektrum bölgeleri için geliştirmiştir.Ry = 3.29 x 1015 1/s
9. Sayfa
SpektroskopiGazların Emisyon SpektrumuNa, Hg, He, H emisyonlarıNote: not all colors are present.Gazların Absorbsiyon Spektrumu
10. Sayfa
Bohr Atom ModeliVarsayımlar: 1. Elektronların yörünge yarıcapı sadece belirli değerler alır. Bu yörüngede kaldığı sürece ışıma yapmaz. (Kararlı durum hipotezi) 2. Elektron enerjisi daha düşük bir yörüngeye geçiş yaptığında frekansı = E / h olan foton yayınlar.Her bir yapıcap beli bir enerjiye karşılık gelir.3. Elektonun dönebileceği yörüngeler kuantlaşmıştır ve açısal momentumun tam katları olmalıdır.
11. Sayfa
Atom SpektrumlarıEmission Spectrum for HydrogenEnergy Levels in HydrogenAbsorption Spectrum For Hydrogen
12. Sayfa
Bohr ModeliBaşarıları: 1. H ve H-benzeri (tek elektronlu) atomların spektrumlarını açıklanabilmiştir. 2. Periyodik çizelgenin genel özelliklerini tanımlayabilmiştir.Başarısızlıkları:Elektronun kararlı yörüngelerde niçin ışıma yapmadığını izah edememiştir.Bohr modeli, çok elektronlu atomların spektrumlarını izah edemez.Atomların manyetik alana konduğundaki hat yarılmalarını açıklayamazSpektral hatların şiddeti hakkında bir şey söyleyemez.Elektonlar yüksek hızlarda hareket etmesine rağmen Bohr modeli relativistik değildir. Bohr Modeli, klasik ve kuantum modelleri arasında “köprü” oluşturur.