İşte Cevaplar
Homojen Karışımlar (Çözeltiler): Her yerinde aynı özelliği gösteren karışımlara homojen karışım denir. Homojen karışımlar bir maddenin başka bir madde içinde çözünmesi ile oluşur. Bu nedenle homojen karışımlara çözelti denir.
Çözeltiler çözücü ve çözünenden oluşur.
Çözücü: Genellikle miktarı fazla olan madde çözücüdür. Su her zaman çözücü sayılır.
Çözünen: Genellikle miktarı az olan madde çözünendir.
Çözünme Şekline Göre Çözelti Çeşitleri:
ÖR: C2H5OH, C12H22O11
İyonik Çözelti: Maddenin çözücü içinde iyonlarına ayrışarak homojen dağılmasıdır. İyonik bileşikler iyonik çözünme gösterir.
ÖR: NaCl, Ca(NO3)2...
İyonik çözeltiler elektriği iletir, bunlara elektrolit çözelti denir. Moleküllü çözeltiler ise elektriği iletmez, bunlara elektrolit olmayan çözeltiler denir.
Çözünen Madde Miktarına Göre Çözelti Çeşitleri Doymuş Çözelti: Belirli sıcaklıkta çözebileceği maksimum miktarda maddeyi çözmüş çözeltilerdir.
Doymamış Çözelti: Belirli sıcaklıkta çözebileceği maksimum miktardan daha az çözünen içeren çözeltilerdir.
Aşırı Doymuş Çözelti: Belirli sıcaklıkta çözebileceği maksimum miktardan daha fazla çözünen içeren çözeltilerdir. Aşırı doymuş çözeltiler kararsızdır. Bir dış etki ile çözünen fazla madde çöker.
Çözünen/Çözücü Oranına Göre Çözelti Çeşitleri
Derişik Çözelti: Çözünen miktarı görece fazla olan çözeltilerdir.
Seyreltik Çözelti: Çözünen miktarı görece az olan çözeltilerdir.
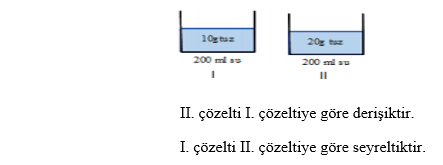
Çözeltiler karıştırıldığında iki çözeltinin arasında bir yoğunlukta yeni karışım elde edilir.
ÇÖZÜNME OLAYI
- Çözünme olayı iyonik ve moleküler olmasının yanı sıra, ısı alış verişi bakımından endotermik (ısı alan) ve ekzotermik (ısı veren) olabilir.
- Çözünme olayı sırasında harcanan enerji, açığa çıkan enerjiden büyükse çözünme olayı ekzotermik, açığa çıkan enerjiden küçükse çözünme olayı endotermiktir.
- Katı ve sıvıların çözünmesi genellikle endotermik, gazların çözünmesi ise genellikle ekzotermiktir.
Hidrasyon ve Solvasyon Bir maddenin suda çözünmesi olayına hidrasyon (hidratasyon), sudan farklı bir çözücüde çözünmesi olayına solvasyon (solvatasyon) adı verilir.
Polarlığın Çözünmedeki Rolü Benzer benzeri çözer ilkesi: Polar maddeler polar çözücülerde, apolar maddeler apolar çözücülerde iyi çözünür. Bir molekülün polarlığı arttıkça çözünme miktarı artar. İyonik katılar polar çözücülerde iyi çözünür.
CCl4, CH4, C2H6, C6H6, CO2, I2 gibi maddeler apolar moleküllerdir. Bu maddelerin biribiri içinde iyi çözünmesi beklenir.
H2O (su), CHCl3 (kloroform), H2S, HF, C2H5OH (etil alkol), gibi maddeler polar moleküllerdir. Bu maddelerin birbiri içinde iyi çözünmesi beklenir.
NaCl, NaOH, Na2CO3 gibi maddeler iyonik katıdırlar ve polar çözücülerde iyi çözünürler.
CCl4 - H2O, C6H6 - CHCl3 gibi ikili karışımlarda moleküller birbirini iyi çözmez.
Çözünme Olayı ve Kimyasal Değişim
İyonik katılar, asitler, O2 gazı ve çoğu kovalent bileşik suda fiziksel yolla çözünürken, CO2 gazı ve Na, K gibi aktif metaller suda kimyasal yolla çözünür.
Ca(NO3)2(k) → Ca2+ + 2NO- 3(suda) (fiziksel çözünme)
CO2 + H2O → H2CO3 → HCO-3 + H+ (kimyasal çözünme)
Na + H2O → NaOH + H2 (kimyasal çözünme)
Diğer Cevaplara Gözat
